La radioactivité est présente dans tout ce qui nous entoure.
Certains rayonnements sont générés naturellement par certains matériaux terrestres : on parle alors de radioactivité tellurique. Mais certains rayonnements viennent également d’au-delà de l’atmosphère. On parle dans ce cas de radioactivité cosmique.
Nous baignons ainsi en permanence dans les rayonnements ionisants dus à la radioactivité naturelle, et ce sans problème pour notre santé.
Les dangers liés à la radioactivité et aux rayonnements ont été découverts au fur et à mesure de son utilisation médicale ou industrielle, avec parfois des conséquences graves sur la santé. Aujourd’hui, l’utilisation de la radioactivité est donc très encadrée.
On appelle radioprotection l’ensemble des dispositions prises, pour assurer la protection de l’homme et de son environnement contre les effets néfastes des rayonnements ionisants.
1- L’atome
Pour expliquer le phénomène de la radioactivité, il est nécessaire d’introduire quelques notions de physique sur l’atome.
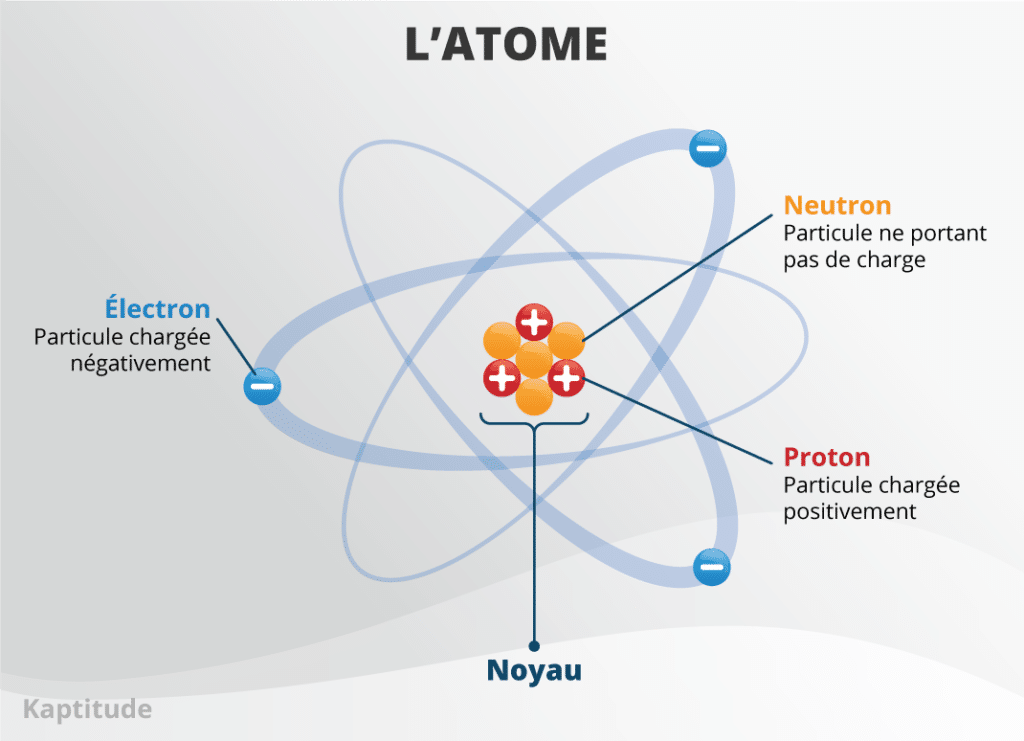
L’atome est constitué d’une partie centrale (le noyau) et d’un nuage périphérique d’électrons.
Le noyau est lui-même constitué d’un ensemble de particules : les protons et les neutrons.
Des trois éléments constituant l’atome, seul le neutron ne porte pas de charge électrique. Il est neutre, d’où son nom.
Un proton quant à lui porte une charge positive et un électron, une charge négative.
Un atome dans son état normal comprend autant de protons que d’électrons. La charge est donc nulle. La masse des électrons est négligeable ! À l’inverse, les protons et les neutrons, de masse à peu près équivalente, sont mille fois plus lourds que les électrons.
La masse d’un atome correspond donc essentiellement à la masse du noyau, c’est-à-dire aux protons et neutrons le constituant.
2- Le numéro atomique et le nombre de masse
Un atome est symbolisé par une ou deux lettres, par exemple H pour Hydrogène ou Cu pour Cuivre.
Le chiffre en bas à gauche indique le nombre de protons caractéristique de cet atome.
On l’appelle le numéro atomique « Z ».
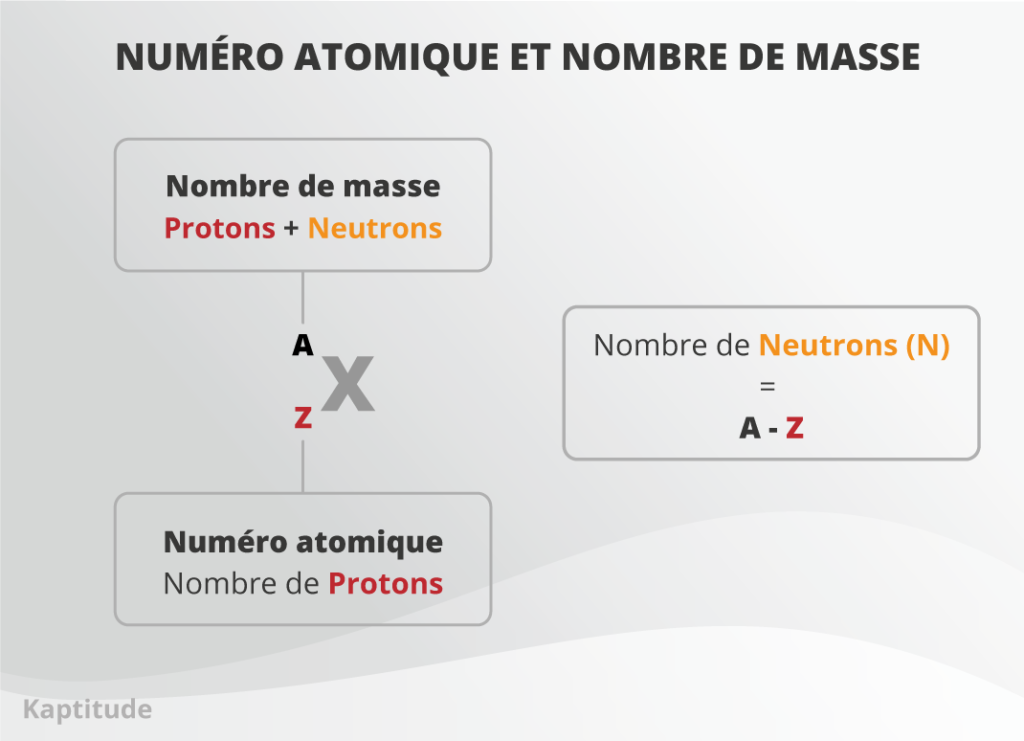
Le chiffre en haut à gauche est appelé nombre de masse “A”. Il correspond à la somme de protons et de neutrons de l’atome.
Le nombre de neutrons est donc égal au nombre de masse A moins le numéro atomique Z.
3- Les isotopes
Le nombre de protons détermine les propriétés chimiques des atomes.
Le tableau périodique des éléments permet de regrouper les atomes par famille, selon leur nombre de protons. On appelle les atomes ayant le même nombre de protons des isotopes et une famille d’isotopes sera appelée « élément chimique ».
Pour exemple, prenons le plus petit élément chimique, l’hydrogène !
Au sein de la famille Hydrogène, il y a 3 membres.
Leur point commun est qu’ils ne possèdent qu’un seul proton : Z=1.
Cela leur confère les mêmes propriétés chimiques : les propriétés de l’hydrogène.
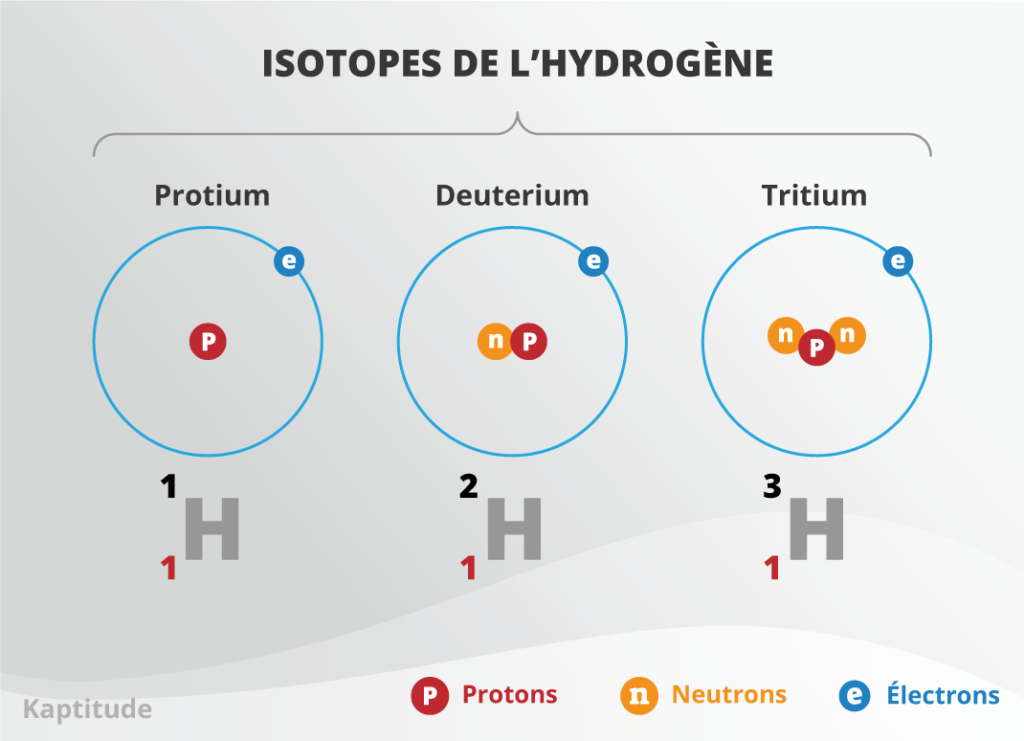
Ils diffèrent cependant par le nombre de neutrons :
- L’hydrogène-1 (Protium) n’a pas de neutron : le proton est tout seul
- L’hydrogène-2 (Deuterium) a un neutron et un proton
- L’hydrogène-3 (Tritium) a deux neutrons et un proton
L’hydrogène-1 étant constitué d’un seul proton et d’un seul électron, il est ainsi le plus léger atome existant
4- Transformation radioactive
Le tritium, qui possède deux neutrons et un proton dans son noyau, est le seul isotope radioactif de la famille. En effet, avec ses deux neutrons pour un proton, son noyau est instable.
Un noyau instable va tendre spontanément vers un état plus stable. On appelle ce phénomène une transformation radioactive.Cette transformation s’accompagne de l’émission de rayonnements α, β ou γ, porteurs d’énergie.
Ces rayonnements iront eux-même interagir avec la matière qu’ils traverseront.
Par un phénomène de désintégration, le noyau va tout d’abord changer de structure.
Le noyau initial (X) perd sa radioactivité après avoir émis son rayonnement.
Il se transforme alors en un autre noyau Y, c’est-à-dire en un nouvel élément chimique.
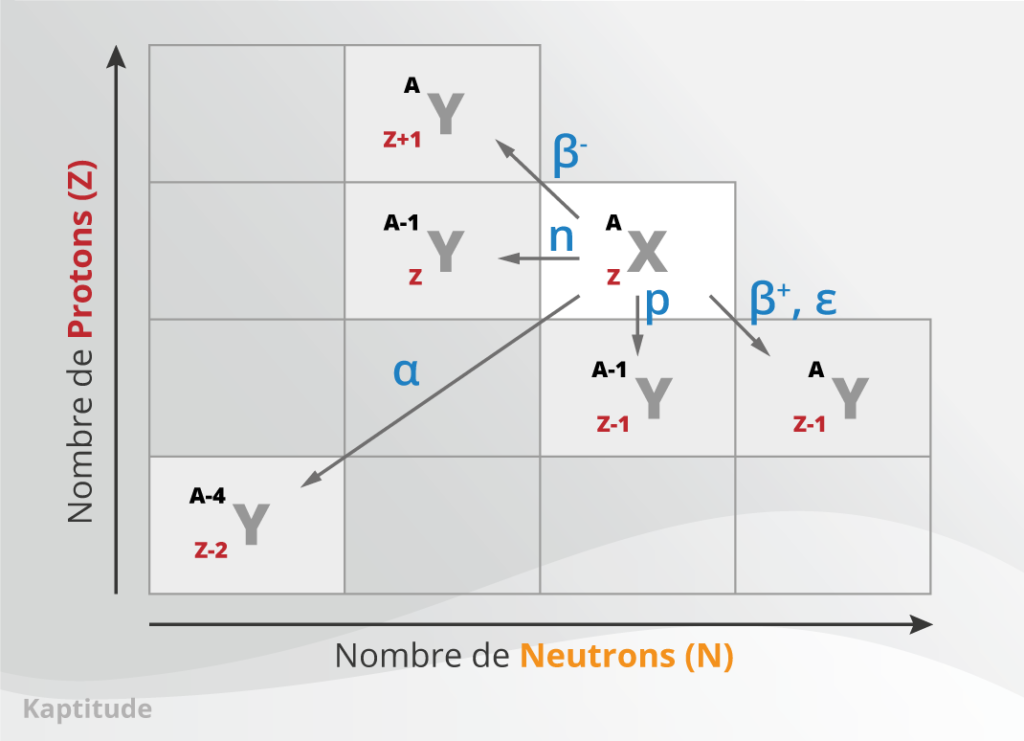
Le noyau Y généré peut éventuellement être encore dans un état excité après cette désintégration. Dans ce cas, il doit perdre de l’énergie pour revenir à un état stable.
La désintégration sera alors suivie d’une désexcitation.
Dans cette seconde étape de désexcitation, de l’énergie est à nouveau libérée mais cette fois-ci, sans modification supplémentaire de structure.
Il faut préciser cependant que la désexcitation ne concerne pas tous les noyaux radioactifs. Et pour ceux concernés, elle apparaîtra toujours à la suite d’une désintégration, c’est-à-dire après le changement de structure nucléaire.
Dans tous les cas, les transformations radioactives s’accompagnent de l’émission de rayonnements.
Il est bon de rappeler que l’ensemble de ce phénomène physique est un phénomène naturel ! Il a été découvert en 1896 par Henri Becquerel qui étudiait alors la phosphorescence et c’est Marie Curie qui a largement contribué à sa caractérisation et l’a nommé « radioactivité ».